Eksamenstest
Niveau: 12
Du får dannet 2 mol vand på gasform. Svaret er 24,8 L/mol. Du skal have fat i idealgasligningen V = nRT/p, hvor du indsætter n = 1 mol, T = 298 K og p = 100.000 Pa. Select all that apply: Dette er en klassisk syre/basereaktion som giver salt vand. Select all that apply: Svaret er 0,3. Saltsyre (HCl) er en stærk syre som afgiver ALLE H<sup> </sup>-ioner til vand. Vi kan derfor antage at den aktuelle stofmængdekoncentration af H<sup> </sup> er den samme som den formelle koncentration af HCl, altså [H<sup> </sup>] = 0.5 mol/L. Derefter beregner vi blot pH som -log([H<sup> </sup>]). Brug formlen for vands ionprodukt. Du kender [[H<sub>3</sub>O<sup> </sup>]] og skal så bare isolere [OH<sup>-</sup>]. Svaret er 1,0 x 10<sup>-12</sup>. Nitrogen har det kemiske symbol N. Det er nummer 7 i det periodiske system og har derfor syv protoner. Svaret er 7. Der er syv protoner og syv neutroner, som alle har en masse på cirka 1.

#1. Hvilken type organisk molekyle vises her?

#2. Hvilken type organisk molekyle vises her?
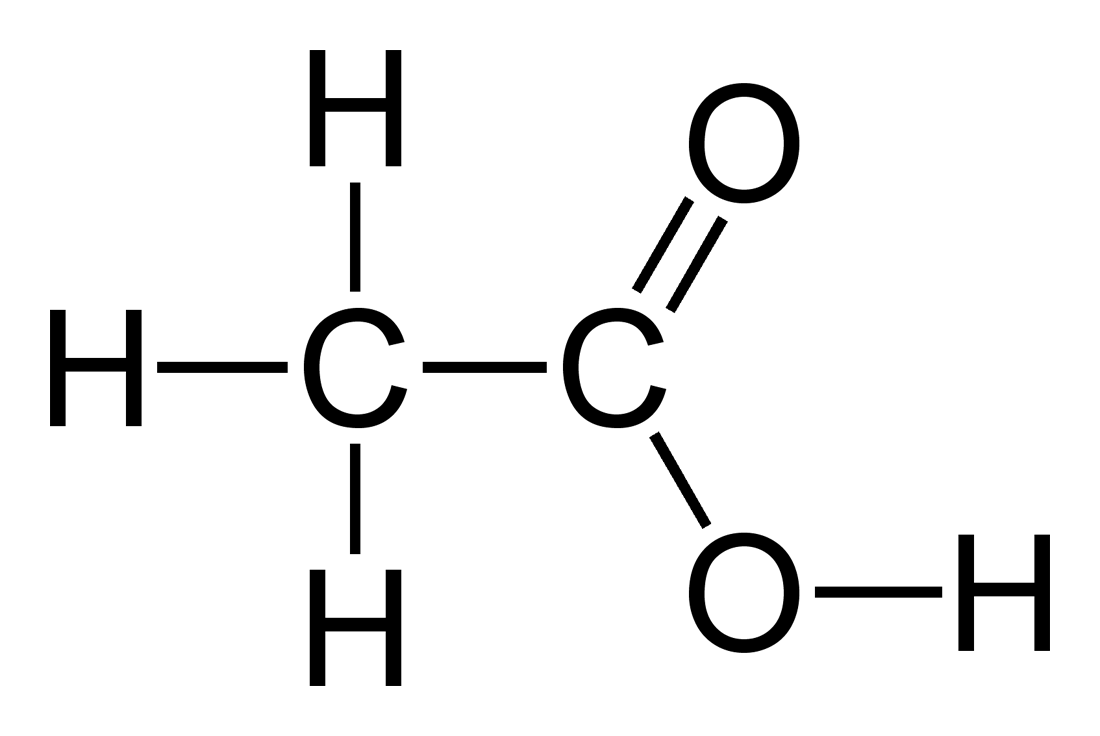
#3. Hvilken type organisk molekyle vises her?
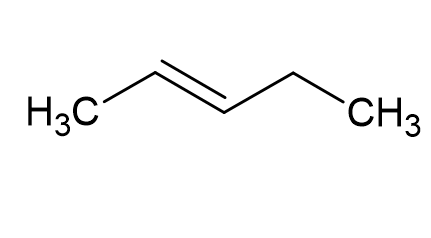
#4. Hvad er molekylets navn?

#5. Hvad er molekylets navn?

#6. Afstem reaktionsskemaet og angiv koefficienterne.
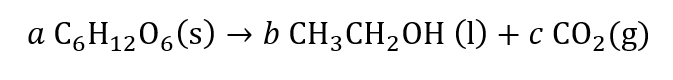
#7. Afstem reaktionsskemaet og angiv koefficienterne.
#8. Den formelle stofmængdekoncentration af HCl i en opløsning er 1 mol/L. HCl opløses i disse mængder fuldstændigt i vand. Hvad er den aktuelle stofmængdekoncetration af HCl? Angiv dit svar i enheden mol/L.
#9. Du opløser 10 g NaCl i 500 mL vand. Hvad bliver massekoncentrationen af NaCl i g/L?
#10. Du opløser 10 g NaCl i 500 mL vand. Hvad bliver stofmængdekoncentrationen af NaCl i mol/L? Afrund dit svar til første decimal.
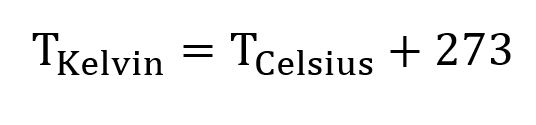
#11. Omregn temperaturen 100 grader celsius til den tilsvarende temperatur i Kelvin. Afrund til nærmeste heltal.

#12. Betragt forbrændingen af dihydrogen. Du har sammenlagt 3 mol gaspartikler inden forbrændingen finder sted, henholdsvis 2 mol H2 og 1 mol O2. Hvor mange mol gas har du, når reaktionen er løbet til ende?
#13. Hvad er volumenet af 1 mol gas ved atmosfærisk tryk og temperatur (p = 100.000 Pa og T = 298K)? Angiv dit svar i liter med første decimal.

#14. Betragt vands syre-basereaktion med sig selv (autohydronolyse). Hvad er koncentrationen af H+ i rent vand i enheden mol/L?
#15. Udpeg de korresponderende syre/base-par:
#16. Du skal kende tre stærke syrer på kemi C. Hvilke?
#17. Svage syrer er svage fordi:
#18. Hvad er produktet af følgende reaktion: H2SO4(aq) + Mg(OH)2(aq)?
#19. Udpeg aller stoffer som giver opløsninger med pH større end 7
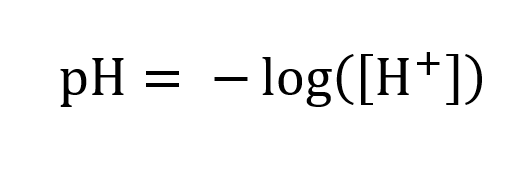
#20. Beregn pH i en saltsyreopløsning med en koncentration på 0,5 mol/L. Angiv dit svar til første decimal.

#21. Beregn [OH-] i en opløsning med en oxoniumkoncentration på 0,01 mol/L. Angiv dit svar som et heltal.
#22. Hvor mange protoner er der i et nitrogen-atom?
?
Find det kemiske symbol for nitrogen og find dets placering i det periodiske system.
#23. Hvor mange neutroner er der i nitrogen-14?
?
14 er massen af nitrogen-isotopen. Du ved, at kun protonerne og neutronerne tæller med i massen. Du ved også, hvor mange protoner der er i et nitrogen-atom. Hvor mange neutroner kan der så være?
#24. Hvilken ion danner calcium
#25. Hvilken ion danner aluminium?

