Kapitel 1.3
Ædelgasreglen
Molekyler og ioner (ædelgasreglen er nedenfor)
Nu har du hørt om grundstofferne. Dem er der som sagt kun halvfems forskellige af i naturen. Men der er jo meget mere end halvfems forskellige stoffer i verden omkring os. Smør, bildæk og striksokker er fx ikke grundstoffer. Gummiet i bildækket består af forskellige grundstoffer som er sat sammen med hinanden. Og det er netop dét en kemiker gør! Altså, sætter grundstoffer sammen!
Man kan sætte grundstoffer sammen på tre forskellige måder, og der er et system i hvilke stoffer der kan sættes sammen med hvilke andre. Du kommer nu til at høre nogle ord som først bliver forklaret om lidt, men du har godt af at få et samlet overblik: 1) Metaller der binder til hinanden, laver metal-bindinger 2) Ikke-metaller der binder til hinanden, laver kovalente bindinger og 3) metaller der binder til ikke-metaller danner ionbindinger.
Metal-bindingerne er ikke så vigtige i gymnasiet, så dem tager vi til sidst. Til gengæld er kovalente bindinger og ionbindinger så vigtige at du ikke kan trække et eneste eksamensspørgsmål uden at skulle tale om mindst én af dem. Her kommer de korte forklaringer: Kovalente bindinger opstår, når to atomer deler to elektroner med hinanden. Ionbindinger opstår når et atom stjæler én eller flere elektroner fra et andet atom.
Dét var forklaringerne, men du ved selvfølgelig stadig ikke nok til helt at forstå dem. Vi bliver derfor nødt til at se grundigere på både de kovalente bindinger og ionbindingerne. Begge bindingstyper opstår imidlertid på grund af samme underlige kendsgerning; nemlig at alle atomer gerne vil have lige så mange elektroner i sin yderste skal som den nærmeste ædelgas. Denne kendsgerning er så vigtigt at den har fået sit eget navn. Vi kalder den ædelgasreglen.
Ædelgasreglen (oktetreglen)
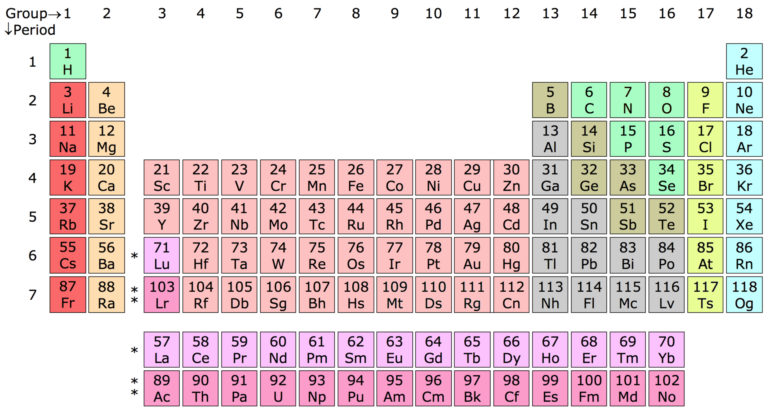
Ædelgasreglen siger at alle atomer gerne vil have lige så mange elektroner i sin yderste skal som den nærmeste ædelgas. Du kan tænke på ædelgasserne som rockstjernerne i det periodiske system: Alle de andre vil gerne ligne dem. Hvis du kigger på det periodiske system, så finder du ædelgasserne i hovedgruppe 8 (altså i kolonnen længst til højre, nogle gange også kaldet gruppe 18). Ædelgasserne omfatter således blandt andet helium (He), neon (Ne) og argon (Ar).
Lad os kigge på klor (Cl) som et eksempel. Klor er i hovedgruppe 7. Klor har altså syv elektroner i sin yderste skal. Den nærmeste ædelgas er argon som har otte elektroner i yderste skal. Klor drømmer derfor om at få en ekstra elektron så den kommer til at ligne argon.
Ædelgasserne har næsten alle sammen otte elektroner i den yderste skal. Derfor bliver reglen ofte kaldt ”oktetreglen” (oktet kommer at græsk ”octa” som betyder otte). Dog har helium kun to elektroner, men den er stadigvæk en ædelgas. Derfor foretrækker de fleste kemilærere at kalde reglen for “ædelgasreglen” i stedet for “oktetreglen”.
Mere behøver du ikke vide om ædelgasreglen. Du er helt normal hvis du synes det virker underligt at alle grundstoffer gerne vil ligne ædelgasserne. Det har også undret mange kemikere. I dag kan kemikere som er gode til matematik regne på at det giver mening, og du må stole på dem – du har ikke en chance for at forstå det som gymnasieelev!
Jeg ved at du nu spørger dig selv: Hvad kan et grundstof mon gøre for at komme til at ligne sin nærmeste ædelgas? Jo, nu skal du høre: de binder sig til hinanden. Enten ved at lave kovalente bindinger eller ion-bindinger. Lad os begynde med ionbindingerne i næste sektion.