Kapitel 1.4
Ioner og ionbindinger
Ioner er atomer der har fået eller mistet elektroner
Aflys din tid ved tandlægen, rul gardinerne ned, sluk telefonen og spids ørerne, for nu bliver det vigtigt. Ionbindinger skal du forstå. Hvis du læser koncentreret de næste fem minutter er du i mål.
Ioner opstår når ét grundstof afgiver én eller flere elektroner til et andet grundstof. Denne overførsel af elektroner sker på grund af ædelgasreglen: Atomer giver og optager elektroner for at komme til at ligne deres nærmeste ædelgas. Det er altid et metal som afgiver elektroner og et ikke-metal som modtager.
Husk at rene grundstoffer altid har lige mange protoner og elektroner og derfor har en samlet elektrisk ladning på nul. Men når et grundstof afgiver en elektron, så bliver atomet efterladt med én proton mere end der er elektroner. Derfor får atomet en positiv ladning. Et atom med en ladning kalder vi for en “ion”.
Lad mig gøre det helt klart for dig hvorfor atomet får en ladning ved at bruge natrium som eksempel. Natrium er grundstof nummer 11 og har derfor elleve protoner og elleve elektroner. Den samlede ladning af et natrium-atom er derfor 11-11 = 0 (jeg tager blot antallet af positive protoner og minusser antallet af negative elektroner). Når natrium mister en elektron, er der kun 10 elektroner tilbage, men antallet af protoner er uændret. Derfor bliver ladningen af atomet nu 11-10 = +1.
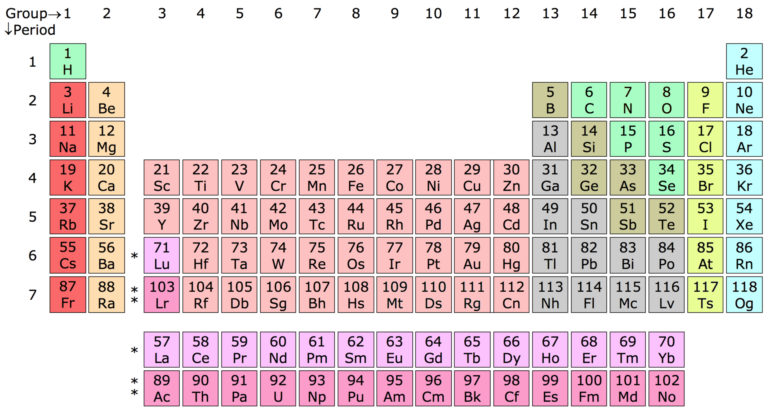
Omvendt bliver et atom negativt ladet når det modtager en elektron. Eksempel: Klor har som grundstof sytten protoner og sytten elektroner (yes, du gætter rigtigt; klor er nr. 17 i det periodiske system). Når klor reagerer med natrium, får klor en ekstra elektron. Derfor bliver ladningen 17-18 = -1.
Nu kommer en af de vigtige pointer: Positive og negative ladninger tiltrækker hinanden. Derfor er det positive natrium-atom tiltrukket af det negative klor-atom. Den elektriske tiltrækning er så stærk, at natrium-ionen og klor-ionen kommer til at hænge sammen; de binder sig til hinanden, og det er denne binding som vi kalder for en ionbinding.

Hvorfor ordet ”ion”? Det er såmænd bare et fint ord for ”Et atom med en ladning”.
Man skal altid angive ladningen når man skriver de kemiske symboler. Man angiver ladningen med hævet skrift. Således skriver man en natrium-ion som Na+ og en klor-ion som Cl–.
Negative ioner får desuden endelsen ”-id”. Man siger derfor ”klorid-ion” om Cl– og ikke “klor-ion”.
Hvorfor opstår ionbindinger
Det korte svar: På grund af ædelgasreglen.
Det lange svar: Stadig “ædelgasreglen”, men jeg må hellere vise hvordan.
Nu fortalte jeg dig ovenfor, at natrium danner ionen Na+ ved at smide en elektron. Men hvorfor vil natrium overhovedet smide en elektron? Det vil den, fordi den derved kommer til at få lige så mange elektroner i sin yderste skal som den nærmeste ædelgas, neon (Ne).
Det ser vi helt tydeligt når vi ser på strukturen af et natrium-atom.
Prøv selv at finde natrium i det periodiske system og tegn atomet.
Du tegnede rigtigt hvis din tegning ligner figuren nedenfor.
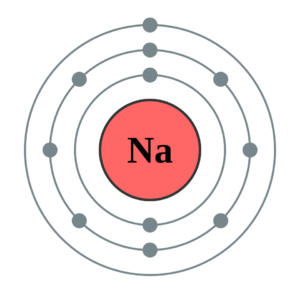
Vi ser at natrium har elleve elektroner i alt fordelt på tre skaller med en enkelt elektron i den yderste skal (natrium er grundstof nr. 11 og findes i periode 3, hovedgruppe 1). Vi ved fra ædelgasreglen at alle atomer gerne vil ligne deres nærmeste ædelgas. Natrium er grundstof nr. 11 i det periodiske system og de nærmeste ædelgasser er derfor neon (nr. 10) og argon (nr. 18). Tydeligvis er natrium tættest på neon. Neon har kun ti elektroner. For at ligne neon, må natrium derfor smide en elektron. Når natrium smider en elektron, bliver natrium efterladt med et overskud af positiv ladning på +1 (fordi der er elleve protoner, men kun ti elektroner).
Voila! Nu har vi brugt ædelgasreglen til at argumentere for hvorfor natrium danner ionen Na+.
Lad os udnytte succesen og finde ud af hvilken ion grundstoffet magnesium vil danne.
Prøv at gøre det for dig selv ved at stille følgende spørgsmål i denne rækkefølge:
1) Hvor er magnesium i det periodiske system?
2) Hvor mange elektroner har magnesium?
3) Hvad er den nærmeste ædelgas?
4) Hvor mange elektroner har den nærmeste ædelgas?
5) Hvor mange elektroner skal magnesium have/afgive før den har lige så mange elektroner som den nærmeste ædelgas?
6) Hvad bliver ladningen på magnesium-ionen når den har lige så mange elektroner som den nærmeste ædelgas?
Her er mine svar: 1) Magnesium er grundstof nr. 12 2) Magnesium har derfor tolv elektroner 3) Den nærmeste ædelgas er neon som er nr. 10 4) Neon har ti elektroner 5) Magnesium skal derfor afgive to elektroner for at ligne neon 6) Magnesium har nu tolv protoner, men kun ti elektroner og ladningen på magnesium-ionen bliver derfor 12-10 = +2. Vi skriver Mg2+.
Fra nu af bliver det piv-nemt: Natrium er i hovedgruppe 1 og dannede ionen Na+. Magnesium er i hovedgruppe 2 og danner ionen Mg2+. Aluminium er i hovedgruppe 3 og danner ionen… Al3+!
Kalium er i hovedgruppe 1. Hvilken ion tror du den danner?
Du har helt ret: kalium bliver til K+. Du kan komme frem til svaret ved at bruge de seks spørgsmål ovenfor. Men hvis bare du forstår at bruge spørgsmålene, må du gerne bruge denne genvej fremadrettet: ”atomer i hovedgruppe 1, 2 og 3 danner ioner med ladningerne 1, 2 og 3”.
En lignende regel gælder for de negative ioner, men her er der lidt mindre slam-bam over ordlyden: ”Atomer fra hovedgruppe 5, 6 og 7 danner ioner med ladningerne -3, -2 og -1”. Lad mig for en god ordens skyld demonstrere reglen med oxygen som eksempel. Hvilken ion vil oxygen (O) danne? Jeg bruger igen de seks spørgsmål ovenfor, nu bare med oxygen i stedet for magnesium. Gå selv tilbage og genlæs og besvar spørgsmålene nu. Mine svar er:
1) Oxygen er grundstof nr. 8 2) Oxygen har derfor otte elektroner 3) Den nærmeste ædelgas er neon som er nr. 10 4) Neon har 10 elektroner 5) Oxygen skal derfor have to elektroner for at ligne neon 6) Oxygen har nu otte protoner, men ti elektroner og ladningen på oxygen-ionen bliver derfor 8-10 = -2. Vi skriver O2-.
Okay, lad os runde dette vigtige afsnit af med en sidste ultra-vigtig pointe: Vi har set at natrium ifølge ædelgasreglen vil smide en elektron. Men hvordan gør den det? Der findes jo ingen skraldespande for overskydende elektroner… Omvendt ville oxygen gerne have to elektroner for at leve op til ædelgasreglen. Men der findes heller ingen elektron-butikker hvor et atom kan gå hen og købe to elektroner.
Så hvad gør atomerne for at leve op til ædelgasreglen?
Har du gættet det?
Ja! De giver og tager elektroner fra hinanden. Derved danner de en ionforbindelse. Lad os blive ved natrium og oxygen: Der skal to natrium-atomer til for at give de to elektroner som oxygen gerne vil have. Resultatet bliver ionforbindelsen natriumoxid, Na2O:
4 Na(s) + O2(g) → 2 Na2O(s)
Her betyder (s) at natrium er et fast stof (fra engelsk: solid) og (g) at oxygen er en gas.
Alle metaller kan danne ion-forbindelser med alle ikke-metaller (der er undtagelser, men det skal du ikke bekymre dig om). Det vil altid ske på den måde at atomerne danner ioner som lever op til ædelgasreglen og resultatet vil altid blive en ionforbindelse med neutral ladning.
Eksempel: Magnesium danner ionen Mg2+ og nitrogen danner ionen N3-. Hvordan kan de tilsammen danne en neutral ionforbindelse? Det kan de ved at tre magnesium-atomer giver sammenlagt seks elektroner til to nitrogen-atomer. Resultatet bliver magnesiumnitrid Mg3N2.
3 Mg(s) + N2(g) → Mg3N2(s)