Kapitel 1.5
Iongitre og sammensatte ioner
Iongitre
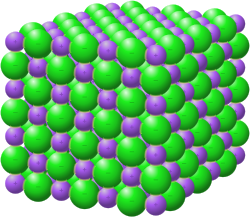
Lad os prøve at koble strukturen på atom-niveau til egenskaberne i menneskeskala (det er sådan noget din lærer elsker at høre). Du har sikkert haft flagesalt i hænderne og ved at det er hårdt, men kan knuses mellem fingrene hvis du trykker til. Kan vi forklare dette med udgangspunkt i iongitteret? Det kan vi: I iongitteret sidder ionerne pænt positiv ved siden af negativ og tiltrækker hinanden. De sidder fast, og derfor er saltet hårdt. Men hvis vi virkelig trykker på saltet, kan vi forskyde et lag i iongitteret sådan at positive ioner fra det ene lag kommer i nærheden af positive ioner fra det andet lag. Og det kan de ikke lide! De frastøder hinanden, og derfor går gitteret i stykker: Der bliver revet en flage af saltet (derfor navnet ”flagesalt”).
En anden karakteristisk egenskab ved mange ionforbindelser er, at de kan opløses i vand. Dette er også vigtigt og et meget typisk emne til eksamen. Det forklarer jeg dog først i det senere kapitel om “opløselighed”. Du kan springe videre til det allerede nu hvis du er interesseret. Hvis du ikke ved hvad en sammensat ionforbindelse er, bør du dog læse det næste afsnit først.

Sammensatte ioner
Okay, det er her kemi bliver lidt irriterende: De pæne ioner dannet fra rene grundstoffer som du har set i de ovenstående afsnit, er nemlig ikke de eneste ioner der findes. Der findes også ioner som er sammensat af flere grundstoffer på samme tid. De kaldes ”sammensatte ionforbindelser” og du har ingen forudsætninger for at forstå hvorfor de ser ud som de gør. Men du skal kunne seks af dem udenad. De er vist i tabellen nedenfor:

Bemærk hvordan de negative sammensatte ioner får endelsen ”-at” i stedet for endelsen ”-id” som de negative ioner der ikke er sammensat (fx klorid, Cl–). Dog er hydroxid er undtagelse; den er både er sammensat og har endelsen ”-id”. Der er ikke andet at sige til det end at livet nogle gange er svært og at navne i kemi ikke er skabt af en klarsynet gud.
Heldigvis reagerer de sammensatte ionforbindelser ligesom de andre ioner: De danner neutrale salte ved at binde sig til ioner af modsat ladning så den samlede ladning bliver nul.
Lad os se på reaktionen mellem natrium-ioner og carbonat-ioner som et eksempel. Natrium-ioner har ladningen +1. Carbonat har ladningen -2. Derfor skal der to natrium-ioner til for at neutralisere en carbonat-ion. Vi får derfor saltet Na2CO3.
2 Na+ (aq) + CO32- (aq) → Na2CO3 (aq)
Her betyder (aq) blot, at stofferne er opløst i vand.
En sidste ting: Hvad så med reaktionen mellem ammonium og carbonat, altså to sammensatte ionforbindelser? Ammonium har ladningen +1 og der skal altså to af dem til for at opveje ladningen fra en carbonat. Vi får saltet (NH4)2CO3. Her betyder det sænkede 2-tal bag parentesen at der er to enheder af ammonium.