Kapitel 1.6
Saltes opløseligehed
Dette emne er en vaskeægte klassiker til eksamen. Lad os begynde hjemme i dit køkken: Du ved at køkkensalt kan opløses i vand: Hvis du drysser salt i gryden med kogende pasta, så “forsvinder” saltet.
Saltet forsvinder selvfølgelig ikke, men det bliver omdannet. Der sker nemlig det at ionerne i iongitteret bliver skilt ad. Man skriver reaktionen på denne måde:
NaCl (s) → Na+(aq) + Cl–(aq)
Her betyder (s) at NaCl er på fast form, mens (aq) betyder at ionerne er blevet opløst i vand. Du kan ikke se ionerne, men du kan smage dem og på den måde overbevise dig selv om at de er der.
Du må dog ikke smage på opløsninger i laboratoriet for at undersøge om de indeholder salt. Mange salte ufarlige, men der er også nogle som er giftige. Og så er der nogle med bivirkninger man gerne vil have kontrol over. Fx er kobbersulfat et brækmiddel, mens magnesiumoxid virker afførende.
Hvordan kan man så undersøge om man har salt i en opløsning? Jo; man kan udnytte at forskellige salte har forskellig opløselighed, dvs. forskellige salte er ikke lige gode til at blive opløst i vand. Jeg vil lige straks fortælle dig hvad du skal vide om forskellige saltes opløselighed, men først skal du vide hvorfor mange salte faktisk bliver opløst i vand.
Vand kan opløse mange typer salt
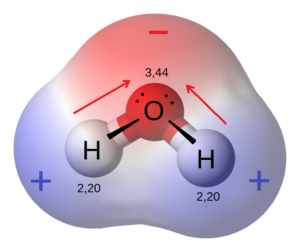
Vandmolekyler er lidt specielle. Samlet set er et vandmolekyle ikke elektrisk ladet, men zoomer man ind på et vandmolekyle, så har det ét område som er svagt negativt ladet og ét område som er svagt positivt ladet. Det kan du se på figuren nedenfor.
Vi bruger ordet “polært” til at beskrive denne egenskab ved vand; altså at vand har to poler med forskellig ladning. Det kan du læse meget mere om i kapitlet “Polaritet” under emnet “Molekyler”, men lige nu er det vigtige bare at vandmolekyler har to elektrisk ladede poler: En negativ pol omkring O-atomet og en positiv pol omkring de to H-atomer.
Se på iongitteret under figuren af vandmolekylet. Forestil dig nu et vandmolekyle nærme sig en positiv ion i iongitteret. Hvordan tror du at vandmolekylet vil vende i forhold til den positive Na+-ion? Læs videre under figurerne når du har tænkt over spørgsmålet – tag dig tid til at kigge på figurerne.

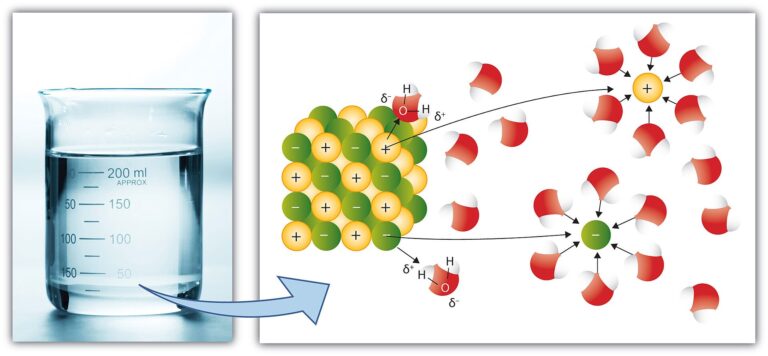
Jo, nu skal du høre: Et vandmolekyle som kommer tæt på en Na+-ion vil selvfølgelig vende med det negative O-atom ind mod Na+-ionen. Husk at positive og negative ladninger tiltrækker hinanden. Det gælder også her: O-atomet fra vandmolekylet vil trække i Na+-ionen, og tiltrækningen kan blive så stor at Na+-ionen bliver revet ud af gitteret. Dette er netop hvad der sker når saltet bliver opløst: Ionerne i ion-gitteret bliver skilt ad fordi vandmolekyler trækker i dem. Du kan se hvordan i figuren nedenfor.
Hvordan tror du et vandmolekyle vil vende sig når det kommer tæt på en negativt ladet Cl–-ion? Her vil vandmolekylet selvfølgelig vende sig sådan at den positive ende med H-atomerne vil pege ind mod Cl–-ionen. Igen vil der være en elektrisk tiltrækning mellem ion og molekyle som gør at ionen kan blive revet løst af gitteret. Saltet går i opløsning!
Det er meget vigtigt at du kan forklare figuren nedenfor til eksamen; altså at du kan forklare hvorfor vandmolekylerne vender som de gør og hvorfor ionerne bliver revet løst fra ion-gitteret.
Let- og tungt-opløselige salte
Det er ikke alle salte som nemt bliver opløst i vand. Og det er faktisk ret nemt at forstå hvorfor. Nu kender du allerede køkkensalt (natriumklorid), og du ved at det er sat sammen af ionerne Na+ og Cl–. Du ved også at dette salt er ret let at opløse i vand.
Prøv nu at se på saltet calciumcarbonat (CaCO3). Det består af ionerne Ca2+ og CO32-. Har du et bud på om dette salt er lige så let at opløse som natriumklorid?
Det er det ikke! Et andet ord for “calciumcarbonat” er “kalk”. Kalk kan ikke opløses i vand (i hvert fald kun i meget små mængder).
Vi kan forklare hvorfor kalk er dårligt opløseligt i vand ved at kigge på ionernes ladning. Jo større ladningsforskellen er mellem ionerne i saltet, jo mere er de tiltrukket af hinanden. I kalk har ionerne ladningerne +2 og -2 (Ca2+ og CO32-). Forskellen er altså 4. Det er en ret stor forskel som betyder at Ca2+-ionerne og CO32--ionerne er stærkt tiltrukket af hinanden. Her kan vandmolekylerne ikke rive ionerne løst af iongitteret.
Lad os sammenligne med køkkensalt, NaCl. Her har ionerne ladningerne +1 og -1. Forskellen i ladning er altså kun 2. Na+ og Cl– er derfor ikke ligeså stærkt tiltrukket af hinanden som ionerne i kalk. Og derfor har vandmolekyler lettere ved at rive dem løs af iongitteret – og derfor er køkkensalt lettere at opløse i vand end kalk.
Det gælder generelt at jo større ladningsforskellen er mellem ioner, jo mindre opløseligt er saltet i vand. Denne tendens ses tydeligt i tabellen nedenfor. Tabellen viser hvilke salte som er let-opløselige (L) og tungt-opløselige (T).