Kapitel 1.9
Elektronprikformler
I forrige kapitel lærte du hvordan man kan vide om to grundstoffer vil danne en kovalent binding eller en ionbinding med hinanden. Nu zoomer vi mere ind på de kovalente bindinger, for du skal på kemi C kunne tegne molekyler og strukturer med kovalente bindinger.
Det er heldigvis ikke så svært. Du skal bare bruge ædelgasreglen og din viden om det periodiske system. I dette kapitel vil jeg vise dig hvordan.
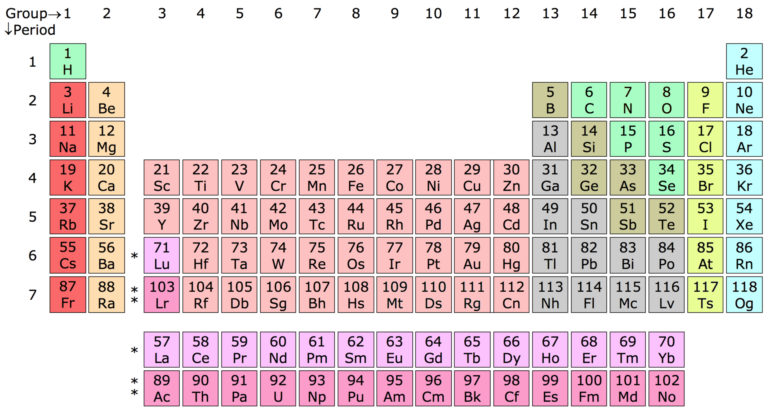
Det lange svar involverer begrebet “elektronegativitet” som lyder værre end det er. I al sin enkelhed er elektronegativitet et tal som ethvert grundstof har som fortæller hvor godt grundstoffet trækker i elektroner.
Flour er det grundstof som er bedst til at trække i elektroner, og det har en elektronegativitet på 4 (helt præcist 3,98). Dernæst kommer oxygen med en elektronegativitet op 3,4.
De dårligste til at tiltrække elektroner er metallerne fra hovedgruppe 1. Fx har natrium (Na) en elektronegativitet på 0,9.
Du kan se en oversigt over de forskellige grundstoffers elektronegativitet i det periodiske system nedenfor.
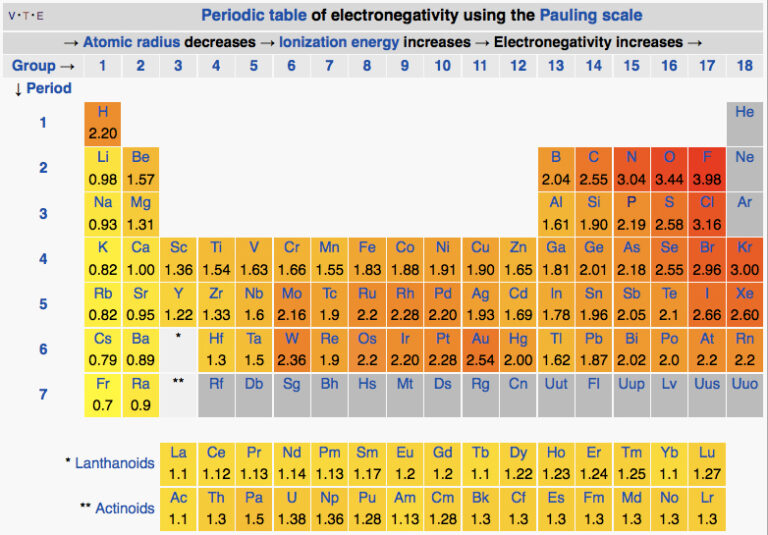
Hvad tror du der sker når et atom med en høj elektronegativitet kommer i kontakt med et atom med lav elektronegativitet? Altså når et atom som trækker kraftigt i elektroner (fx flour) kommer tæt på et, som er dårlig til at holde på sine elektroner (fx natrium)? Ja; så snupper det stærke atom en elektron fra den mindre stærke. Der bliver overført en elektron mellem atomerne. Derved bliver de til ioner og en ionbinding opstår.
Vi kan regne ret præcist hvornår dette sker (pst.: det er det du skal kunne til eksamen). Når forskellen i elektronegativitet mellem to atomer er mere end 1,7, så opstår en ionbinding. Når forskellen er mindre end 1,7, så opstår en kovalent binding; her er de to grundstoffer nemlig cirka lige gode til at trække i elektronerne så her kan den ene ikke stjæle fra den anden.
For nemheds skyld forkorter vi “elektronegativitet” med “EN”. Til at betegne forskelle bruger vi det græske bogstav Δ (udtales “delta”). Vi kan derfor i kort form skrive:
ΔEN > 1,7: Ionbinding
ΔEN < 1,7: Kovalent binding
Når du udregner forskellen skal du altid tage det største tal og trække fra det mindste så du ikke får et negativt tal.
Her kommer et typisk spørgsmål du kan blive stillet i løbet af den mundtlige eksamen i kemi: “Vil calcium og klor danne en ionbinding eller en kovalent binding”?
Prøv selv at svare på spørgsmålet ved at regne på forskellen i elektronegativitet imellem dem – du kan finde elektronegativiteten for calcium (Ca) og klor (Cl) i tabellen figuren ovenfor. Jeg viser dig mit svar nedenfor, men jeg indsætter lige et billede af en vaskebjørn så du ikke ser svaret med det samme.

Her er mit svar: Vi ser at calcium har en elektronegativitet på 1,00 og klor har 3,16. Vi får da forskellen:
ΔEN = EN(Cl) – EN(Ca) = 3,16 – 1,00 = 2,16
Da ΔEN er større end 1,7 må bindingen mellem calcium og klor være en ionbinding.