Kapitel 1.7
Kovalente bindinger
Vil du se en kovalent binding? Så luk øjnene op og se dig omkring. Alt hvad dit blik lander på, består af atomer der er bundet til hinanden med kovalente bindinger (medmindre du lige nu stirrer intenst på en saltkrystal eller et blankt stykke metal. Men det går jeg ud fra at du ikke gør). Maling, vand, hunde, forældre og sofapuder består af kovalent bundne atomer.
En kovalent binding opstår når to atomer deler to elektroner med hinanden. Der er to elektroner i en kovalent binding – derfor kaldes den også en “elektronparbinding”. De to elektroner fungerer som en slags lim mellem de to atomer så de kommer til at hænge sammen. Hvis det bare er få atomer der hænger sammen, så har vi et molekyle. Luft og vand består af molekyler. Hvis vi har en længere kæde eller et helt netværk af atomer der har bundet sig til hinanden, så har vi en kovalent struktur. Det gælder fx for plastic (som også kaldes en “polymer”), træ og glas. Se eksempler på kovalente bindinger i figurerne nedenfor.
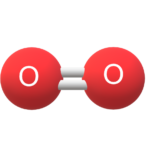
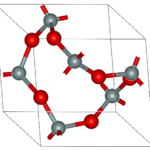
Hvorfor vil atomerne gerne dele elektroner med hinanden? Har du selv et bud?
Du kender svaret, for forklaringen er “ædelgasreglen”. Det er endnu en grund til at du SKAL huske ædelgasreglen.
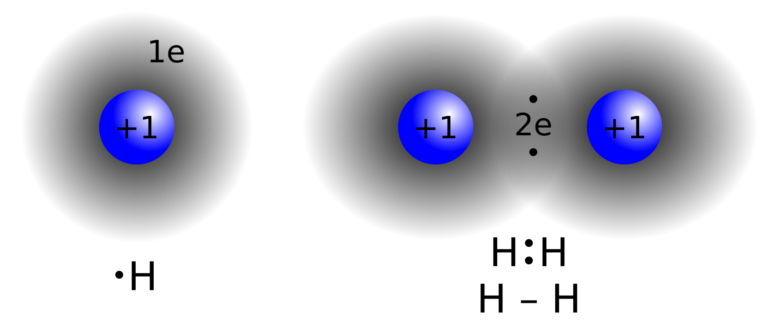
Så lad os genopfriske den meget simple, men meget vigtige ædelgasregel: Reglen fortæller at alle atomer gerne vil have lige så mange elektroner i sin yderste skal som den nærmeste ædelgas. Se molekylet dihydrogen nedenfor som eksempel. Her deler to hydrogen-atomer to elektroner med hinanden. På den måde får de begge atomer elektroner i deres yderste skal ligesom deres nærmeste ædelgas; helium.
Hvis du husker godt, så husker du at vi også brugte ædelgasreglen til at forklare hvorfor der opstår ion-bindinger, altså bindinger hvor et atom giver en eller flere elektroner til et andet atom i stedet for at deles om dem.
Hvordan kan ædelgasreglen forklare både ion-bindinger og kovalente bindinger? Eller sagt på en anden måde: Kan vi vide hvornår to atomer vil danne ionbinding og hvornår de vil danne en kovalent binding til hinanden?
Ja! Det kan vi. Du kan give mig to tilfældige grundstoffer fra det periodiske system, og så kan jeg fortælle dig hvordan de vil binde sig til hinanden. Nu skal jeg fortælle dig hvordan jeg gør det. Svaret har at gøre med hvor godt det enkelte atom tiltrækker elektroner. Det beskriver vi med begrebet “Elektronegativitet”, og det emne er så vigtigt at det fortjener et kapitel for sig selv. Gå roligt videre til næste kapitel.